I. प्रस्तावना: CRISPR क्या है? (Introduction: What is CRISPR?)
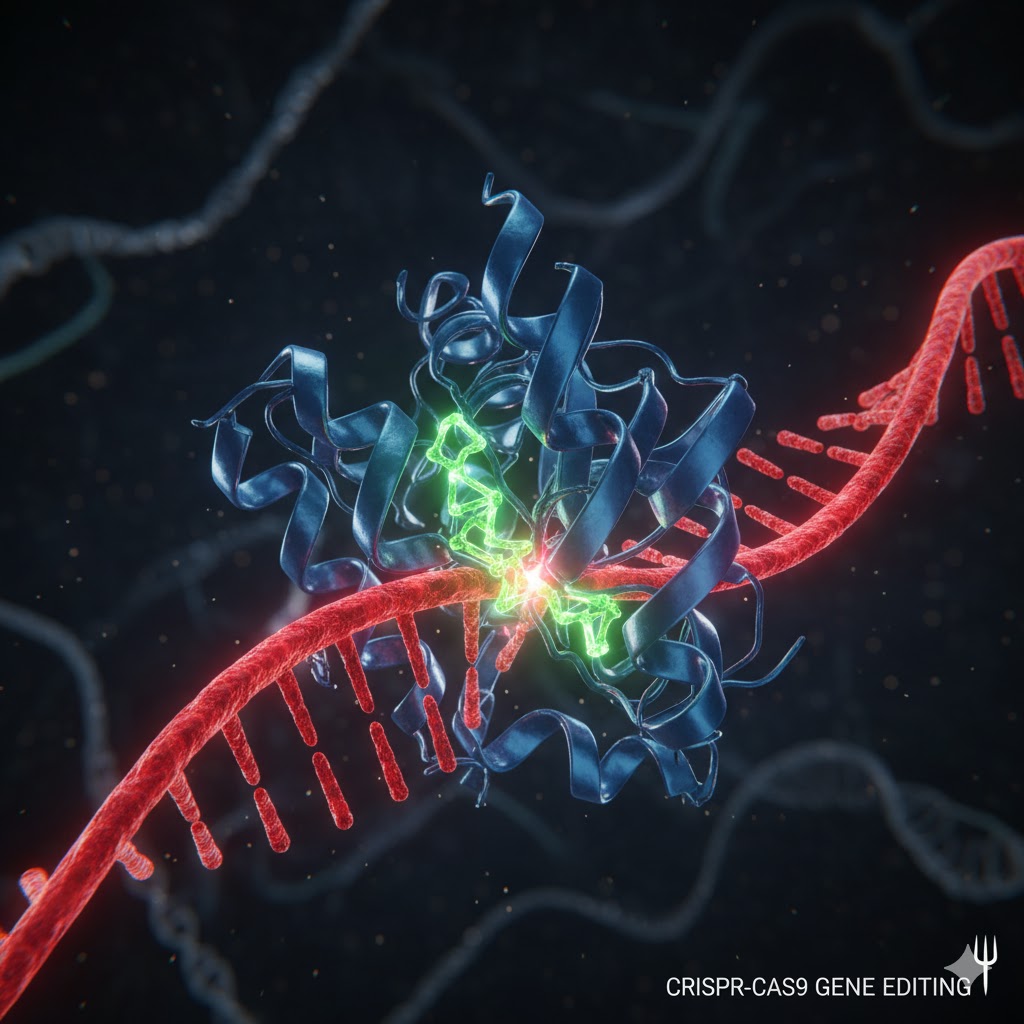
परिभाषा: CRISPR जीन एडिटिंग (Clustered Regularly Interspaced Short Palindromic Repeats) एक क्रांतिकारी जीन एडिटिंग तकनीक है जो वैज्ञानिकों को आनुवंशिक सामग्री (DNA) को अत्यंत सटीकता से बदलने, हटाने या जोड़ने की अनुमति देती है। यह एक ऐसी जैविक प्रणाली है जिसे बैक्टीरिया ने लाखों वर्षों में विकसित किया है, और जिसे अब मानव प्रौद्योगिकी के लिए अनुकूलित (adapted) किया गया है। इसे अक्सर “आणविक कैंची” (Molecular Scissors) कहा जाता है, क्योंकि यह DNA की दोहरी लड़ी को किसी भी वांछित स्थान पर काटने में सक्षम है।
सरल व्याख्या: इस तकनीक की कल्पना एक ऐसे ‘सर्च और रिप्लेस’ (Search and Replace) फंक्शन के रूप में की जा सकती है जो कंप्यूटर प्रोग्राम में कोड बदलने जैसा है, लेकिन यह क्रिया जीवित कोशिकाओं के अंदर, उनके मूल DNA में की जाती है। यह हमें जीवन के मूल ब्लूप्रिंट को फिर से लिखने की शक्ति देती है।
प्रौद्योगिकी का महत्त्व: CRISPR ने आनुवंशिक अनुसंधान के क्षेत्र में क्रांति ला दी है। इसकी सटीकता, गति, और कम लागत के कारण, इसके अनुप्रयोग चिकित्सा, कृषि और जैव प्रौद्योगिकी (Biotechnology) के क्षेत्र में अभूतपूर्व संभावनाएँ पैदा करते हैं, जिसमें लाइलाज बीमारियों का स्थायी इलाज और खाद्य सुरक्षा में सुधार शामिल है।
II. इतिहास और आविष्कार (History and Invention) – कौन और कब?
A. CRISPR की शुरुआत (The Start of CRISPR)
1987: CRISPR की कहानी की शुरुआत तब हुई जब जापान के वैज्ञानिक योशिजुमी इशिन्ो (Yoshizumi Ishino) ने जीवाणु (ई. कोलाई, E. coli) के जीनोम में पहली बार CRISPR जैसे दोहराए जाने वाले DNA अनुक्रमों (Repeated DNA Sequences) की खोज की। उस समय, उन्हें यह नहीं पता था कि ये अजीबोगरीब सीक्वेंस क्या करते हैं और इनका क्या जैविक कार्य है।
2005: वर्षों बाद, फ्रांस के फ्रांसिस्को मोजीका (Francisco Mojica) ने सिद्ध किया कि ये CRISPR सीक्वेंस वास्तव में बैक्टीरिया के अनुकूली प्रतिरक्षा तंत्र (Adaptive Immune System) का एक अभिन्न हिस्सा हैं। ये सीक्वेंस अनिवार्य रूप से पुराने वायरल हमलों की याददाश्त के रूप में कार्य करते हैं, जिससे बैक्टीरिया भविष्य में समान वायरसों से बचाव कर सकता है। मोजीका ने ही सबसे पहले सुझाव दिया कि CRISPR एक रक्षात्मक उपकरण है।
B. ‘आविष्कारक’ और प्रमुख सफलता (The ‘Inventors’ and Major Breakthrough)
2012 (The Breakthrough Year): CRISPR को एक एडिटिंग टूल के रूप में बदलने का सबसे बड़ा वैज्ञानिक कदम इसी वर्ष उठाया गया।
वैज्ञानिक: यह सफलता मुख्य रूप से जेनिफर डोडना (Jennifer Doudna) (कैलिफ़ोर्निया विश्वविद्यालय, बर्कले) और इमैनुएल चारपेंटियर (Emmanuelle Charpentier) (तब स्वीडन में) के संयुक्त प्रयास से मिली।
सफलता: डोडना और चारपेंटियर ने दिखाया कि Cas9 (CRISPR-associated protein 9) नामक एंजाइम के साथ CRISPR को जोड़कर, इसे एक प्रोग्रामेबल टूल में बदला जा सकता है। इसका मतलब है कि इसे किसी भी जीव के DNA को किसी भी वांछित स्थान पर काटने के लिए निर्देशित किया जा सकता है। यह खोज जीन एडिटिंग के लिए एक सटीक, तेज और सस्ता तरीका साबित हुई।

नोबेल पुरस्कार: 2020 में, उन्हें इस अभूतपूर्व कार्य के लिए रसायन विज्ञान में नोबेल पुरस्कार से सम्मानित किया गया, जिससे यह स्पष्ट हो गया कि जीन एडिटिंग विज्ञान और मानवता के लिए कितनी महत्वपूर्ण उपलब्धि है। https://www.nobelprize.org/prizes/chemistry/2020/summary/
III. CRISPR की कार्यप्रणाली और जटिलता (Mechanism and Complexity)
A. उपकरण: Cas9 और गाइड RNA (The Tools: Cas9 and Guide RNA)
Cas9 प्रोटीन: यह वह मुख्य “कैंची” है जो DNA को काटती है। Cas9 वास्तव में एक न्यूक्लियेज एंजाइम (Nuclease Enzyme) है जो DNA की फॉस्फोडिएस्टर बैकबोन को तोड़ने की क्षमता रखता है। https://www.addgene.org/guides/crispr/
गाइड RNA (gRNA): यह वह “डाक कोड” या नेविगेटर है जो Cas9 प्रोटीन को DNA में लक्षित स्थान (Target Location) तक मार्गदर्शन करता है। gRNA लगभग 20 न्यूक्लियोटाइड लंबा होता है। यह लक्षित DNA अनुक्रम के पूरक (complementary) के रूप में डिज़ाइन किया जाता है।
क्रियाविधि: gRNA और Cas9 एक साथ एक कॉम्प्लेक्स बनाते हैं। यह कॉम्प्लेक्स कोशिका के केंद्रक (Nucleus) में प्रवेश करता है। gRNA, DNA के लंबे स्ट्रैंड को स्कैन करता है। जैसे ही gRNA लक्षित DNA अनुक्रम को पहचानता है और उससे जुड़ता है, Cas9 को सक्रिय होने का निर्देश मिलता है, और यह ठीक उसी स्थान पर DNA की दोनों लड़ियों (डबल-स्ट्रैंड ब्रेक) को काट देता है।
B. संपादन की जटिलता (Complexity in Editing)
DNA कटने के बाद, कोशिका इसे जीवन-रक्षक प्रतिक्रिया के रूप में तुरंत ठीक करने की कोशिश करती है। वैज्ञानिक इसी मरम्मत प्रक्रिया का उपयोग वांछित बदलाव लाने के लिए करते हैं।
1. NHEJ (Non-Homologous End Joining): यह कोशिका द्वारा DNA को जोड़ने का सबसे आम और त्रुटि-प्रवण (error-prone) तरीका है। इस प्रक्रिया में, कोशिका टूटे हुए सिरों को बस वापस एक साथ चिपका देती है, लेकिन अक्सर इस दौरान कुछ न्यूक्लियोटाइड खो जाते हैं या जुड़ जाते हैं, जिससे लक्षित जीन अक्षम (Inactivate) हो जाता है (जीन Knockout)।
2. HDR (Homology-Directed Repair): यह सटीक संपादन (Precise Editing) के लिए उपयोग किया जाने वाला तरीका है। इसमें, वैज्ञानिक कटे हुए स्थान के साथ मिलता-जुलता एक टेम्प्लेट DNA (Template DNA) कोशिका को प्रदान करते हैं। कोशिका इस टेम्प्लेट को गाइड के रूप में उपयोग करके कटे हुए स्थान की मरम्मत करती है, जिससे वैज्ञानिक द्वारा डाली गई नई जानकारी को DNA में सफलतापूर्वक जोड़ा जा सकता है।
IV. उपयोग के क्षेत्र और प्रमुख सफलताएँ (Applications and Major Breakthroughs)
A. चिकित्सा और स्वास्थ्य (Medicine and Health)
| क्षेत्र | उपयोगिता (Utility) | प्रमुख सफलता (Major Breakthrough) |
| आनुवंशिक रोग | सिकल सेल एनीमिया (Sickle Cell Anemia), सिस्टिक फाइब्रोसिस और हंटिंगटन रोग जैसे एकल-जीन विकारों का स्थायी उपचार करने की क्षमता। | CRISPR Therapeutics ने रक्त विकारों (Blood Disorders) जैसे सिकल सेल एनीमिया और बीटा थैलेसीमिया का सफल In Vivo (शरीर के अंदर) उपचार किया है, जिससे रोगियों को रोग-मुक्त जीवन मिला है। |
| कैंसर उपचार | T-कोशिकाओं (T-Cells) को आनुवंशिक रूप से संपादित (एडिट) करके उन्हें कैंसर कोशिकाओं को नष्ट करने के लिए अधिक प्रभावी, स्मार्ट हथियार बनाना (जिसे CAR T-Cell Therapy में सुधार कहते हैं)।https://cancerfax.com/hi/crispr-and-gene-editing-revolutionizing-gene-therapy/ | कैंसर के इलाज के लिए CRISPR-आधारित नैदानिक परीक्षणों (Clinical Trials) की शुरुआत हुई है, जहाँ रोगी की T-कोशिकाओं को संपादित करके वापस शरीर में डाला जाता है। |
| वायरल रोग | HIV और हर्पीस जैसे वायरसों के DNA को मानव जीनोम से लक्षित करके हटाना, जो लाइलाज बीमारियों का स्थायी समाधान हो सकता है। | चूहों और अन्य जीवों में HIV के DNA को निष्क्रिय करने में सफलता मिली है, जिससे मनुष्यों में इलाज की उम्मीद जगी है। |
B. कृषि और खाद्य सुरक्षा (Agriculture and Food Security)
बेहतर फसलें: CRISPR का उपयोग करके ऐसी फसलें बनाई जा सकती हैं जो सूखे, अत्यधिक गर्मी और विभिन्न कीटों के प्रति अधिक प्रतिरोधी (Resistant) हों, जिससे वैश्विक खाद्य उत्पादन सुरक्षित हो सके।
तेज विकास और पोषण: CRISPR पारंपरिक प्रजनन (Breeding) की तुलना में बहुत तेजी से अधिक उत्पादन और पोषक तत्वों वाली फसलें (जैसे: फफूंदी-प्रतिरोधी अंगूर, या अधिक विटामिन डी वाले टमाटर) विकसित कर सकती है।
पशुधन: पशुओं को सामान्य रोगों (जैसे स्वाइन फ्लू) से बचाने के लिए उनमें प्रतिरोधक क्षमता बढ़ाना और पर्यावरणीय स्थिरता के लिए मीथेन उत्सर्जन कम करने वाली पशु प्रजातियाँ विकसित करना।
V. उपलब्ध सुविधाएँ और प्रगति में अनुसंधान (Facilities Available and Research in Progress)
उपलब्ध सुविधाएँ (Facilities):
- कई विश्वविद्यालय और निजी कंपनियाँ (जैसे Editas Medicine, Intellia Therapeutics) अब CRISPR-Cas9 और इसके उन्नत रूपों जैसे CRISPR-Cas12 एंजाइमों का उपयोग करके जीन एडिटिंग सेवाएँ प्रदान करती हैं, विशेष रूप से अनुसंधान और दवा विकास के लिए।
- भारत में CSIR-IGIB (Institute of Genomics and Integrative Biology), CCMB (Centre for Cellular and Molecular Biology) और विभिन्न IITs जैसे संस्थान CRISPR अनुसंधान में अग्रणी हैं और छात्रों तथा शोधकर्ताओं को उन्नत सुविधाएँ प्रदान करते हैं।
प्रगति में अनुसंधान (Research in Progress):
- बेस एडिटिंग (Base Editing): यह तकनीक DNA की दोनों लड़ियों को काटने से बचती है, जिससे त्रुटियों का खतरा कम होता है। यह केवल एक न्यूक्लियोटाइड (A, T, C, या G) को सीधे बदलकर वांछित म्यूटेशन को ठीक करती है।
- प्राइम एडिटिंग (Prime Editing): इसे “सर्च एंड रिप्लेस” का सबसे सटीक रूप कहा जाता है। यह लंबी DNA स्ट्रैंड को हटा या बदल सकती है, जिससे जटिल आनुवंशिक म्यूटेशन को भी ठीक किया जा सकता है।
- Cas13: वैज्ञानिक अब Cas13 जैसे एंजाइमों का उपयोग कर रहे हैं जो RNA (DNA नहीं) को लक्षित करते हैं। यह वायरल संक्रमणों के लिए अस्थायी और सुरक्षित उपचार विकसित करने की दिशा में एक बड़ा कदम है।
VI. चुनौतियाँ और जटिलताएँ (Challenges and Complexities)
| चुनौती (Challenge) | विवरण (Description) |
| ऑफ-टारगेट प्रभाव (Off-Target Effects) | यह CRISPR के साथ सबसे बड़ी तकनीकी समस्या है। Cas9 प्रोटीन का अनजाने में DNA के गलत हिस्सों को काट देना (जहां लक्षित अनुक्रम से मिलती-जुलती संरचना हो) अनपेक्षित म्यूटेशन या गंभीर दुष्प्रभाव (Side Effects) पैदा कर सकता है। |
| वितरण (Delivery) | Cas9/gRNA कॉम्प्लेक्स को शरीर के अंदर सही कोशिकाओं तक सुरक्षित रूप से पहुँचाना एक प्रमुख इंजीनियरिंग चुनौती है। इसके लिए अक्सर संशोधित वायरसों (Modified Viruses) या लिपिड नैनोपार्टिकल्स (Lipid Nanoparticles) का उपयोग किया जाता है, जिनकी अपनी सुरक्षा चिंताएँ हैं। |
| नैदानिक लागत (Clinical Cost) | ये जीन थेरेपी बहुत महंगी हैं। उच्च अनुसंधान और विकास लागत के कारण, ये उपचार विकासशील देशों में आम लोगों की पहुँच से बाहर हो जाते हैं, जिससे चिकित्सा समानता (Medical Equity) का मुद्दा पैदा होता है। |
VII. नैतिक जोखिम और हानि (Ethical Risks and Loss to Use)
A. नैतिक जोखिम (Ethical Risks)

जर्मलाइन एडिटिंग (Germline Editing): मानव भ्रूण, अंडे या शुक्राणु (Sperm) में आनुवंशिक परिवर्तन करना, जो अगली पीढ़ियों को विरासत में मिलेंगे। अधिकांश देशों ने इस पर कड़े प्रतिबंध लगाए हैं क्योंकि इससे “डिजाइनर बच्चे” (Designer Babies) बनाने की संभावना पैदा होती है, जिससे गंभीर नैतिक और सामाजिक बहस छिड़ गई है।
समानता (Equity): यदि यह तकनीक केवल धनी व्यक्तियों या विकसित देशों के लिए उपलब्ध है, तो यह स्वास्थ्य और गुणवत्तापूर्ण जीवन के मामले में असमानता (Inequality) को और गहरा कर सकती है, जिससे समाज में आनुवंशिक विभाजन हो सकता है।
B. अनपेक्षित हानि (Unintended Loss/Harm)
अज्ञात दीर्घकालिक प्रभाव: CRISPR-आधारित थेरेपी नई हैं। मानव जीनोम पर किए गए परिवर्तनों के दीर्घकालिक (Long-term) परिणाम अभी तक अज्ञात हैं, और पीढ़ियों तक इनका अध्ययन करना आवश्यक है।
पारिस्थितिकीय जोखिम (Ecological Risk): CRISPR का उपयोग करके बनाए गए जीवों (Genetically Modified Organisms – GMOs) का यदि अनियंत्रित रूप से पर्यावरण में प्रसार होता है, तो यह मौजूदा पारिस्थितिकी तंत्र (Ecosystem) और जैव विविधता पर अप्रत्याशित नकारात्मक प्रभाव डाल सकता है।
VIII. वैश्विक उपयोग और भारत में भविष्य (Global Use and Future in India)
A. वैश्विक उपयोग (Global Landscape)
संयुक्त राज्य अमेरिका: यह देश CRISPR अनुसंधान में वैश्विक नेतृत्व करता है, जिसमें सबसे अधिक नैदानिक परीक्षण (Clinical Trials) चल रहे हैं और निजी कंपनियाँ अरबों डॉलर का निवेश कर रही हैं।
चीन: चीन अनुसंधान में सबसे तेज प्रगति के लिए जाना जाता है, विशेष रूप से मानव भ्रूण एडिटिंग के विवादास्पद प्रयोगों के लिए, जिसने वैश्विक नियमों को सख्त करने की मांग उठाई है।
यूरोप: यूरोपीय संघ ने जर्मलाइन एडिटिंग और कुछ प्रकार के CRISPR-संपादित खाद्य पदार्थों पर सख्त नियामक ढाँचा (Stricter Regulatory Framework) और प्रतिबंध लागू किए हैं।
B. भारत में भविष्य और उपयोगिता (Future in India)
उपयोगिता: भारत में सिकल सेल एनीमिया, थैलेसीमिया और कुपोषण से संबंधित रोगों का बोझ अधिक है। CRISPR भारत के लिए एक गेम-चेंजर हो सकता है, क्योंकि यह इन रोगों का स्थायी और लागत प्रभावी समाधान प्रदान कर सकता है।https://www.youtube.com/watch?v=HGtQzhQJq4Y
सुविधाएँ और अनुसंधान: IGIB, CCMB जैसे भारतीय संस्थान सक्रिय रूप से CRISPR पर शोध कर रहे हैं, विशेष रूप से वायरल निदान (जैसे FELUDA CRISPR-आधारित COVID-19 टेस्ट) और कृषि फसलों में सुधार के लिए।
विनियामक ढाँचा (Regulatory Framework): भारत में आनुवंशिक रूप से संशोधित जीवों (GMOs) और नैदानिक परीक्षणों के लिए एक सख्त नियामक प्रक्रिया है (GEAC – Genetic Engineering Appraisal Committee), जो अनुसंधान और अनुप्रयोगों में सुरक्षा सुनिश्चित करती है।
IX. निष्कर्ष (Conclusion)
CRISPR जीन एडिटिंग केवल एक उपकरण नहीं है; यह जैविक विज्ञान में एक मूलभूत बदलाव है। यह मानवता को बीमारियों को जड़ से खत्म करने, खाद्य सुरक्षा बढ़ाने और जीवन की गुणवत्ता में सुधार करने की अभूतपूर्व शक्ति देता है। हालांकि इसके साथ बड़े नैतिक और सुरक्षा जोखिम जुड़े हैं, विशेष रूप से जर्मलाइन एडिटिंग के संबंध में, लेकिन इसकी क्षमता अपरिमित है। भविष्य के लिए यह आवश्यक है कि इस शक्ति का उपयोग जिम्मेदारी, नैतिकता, सावधानी और वैश्विक सहयोग के साथ किया जाए, ताकि यह सुनिश्चित हो सके कि CRISPR का लाभ समाज के सभी वर्गों तक पहुँचे।
Read this: https://theswadeshscoop.com/punarjanm-ka-rahasya-rebirth/ https://theswadeshscoop.com/theswadeshscoop-com-the-taos-hum-mystery/






